|
2019哈三中高三期末考各科試題及答案向?qū)W霸進(jìn)軍已匯總整理,考題由知名專(zhuān)家結(jié)合了2019高考大綱(考試說(shuō)明)并依托最新時(shí)事為背景出的,通過(guò)此次考試,高三的考生可了解自己的復(fù)習(xí)備考情況,同時(shí)也可以作為2019高考復(fù)習(xí)資料。
2019哈三中高三期末考各科試題及答案目錄一覽 2019哈三中高三期末考(語(yǔ)文科目)試題及答案 2019哈三中高三期末考(數(shù)學(xué)科目)試題及答案 2019哈三中高三期末考(英語(yǔ)科目)試題及答案 2019哈三中高三期末考(物理/化學(xué)/生物)試題及答案 2019哈三中高三期末考(地理/歷史/政治)試題及答案
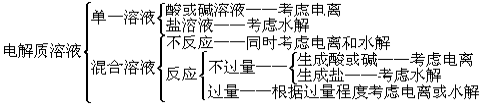
附:高考知識(shí)點(diǎn)之化學(xué)中的守恒知識(shí)匯總加練習(xí) 電荷守恒和物料守恒知識(shí)點(diǎn) 1.電荷守恒:電解質(zhì)溶液中所有陽(yáng)離子所帶有的正電荷數(shù)與所有的陰離子所帶的負(fù)電荷數(shù)相等。如NaHCO3溶液中:n(Na+)+n(H+)=n(HCO3-)+2n(CO32-)+n(OH-)推出: c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) 2.物料守恒:電解質(zhì)溶液中由于電離或水解因素,離子會(huì)發(fā)生變化變成其它離子或分子等,但離子或分子中某種特定元素的原子的總數(shù)是不會(huì)改變的。如NaHCO3溶液中n(Na+):n(c)=1:1,推出:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) 3.導(dǎo)出式——質(zhì)子守恒: 如碳酸鈉溶液中由電荷守恒和物料守恒將Na+離子消掉可得:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。 如醋酸鈉溶液中由電荷守恒和物料守恒將鈉離子消掉可:c(OH-)=c(H+)+c(CH3COOH)。 [規(guī)律總結(jié)]正確的思路:
【常見(jiàn)題型】 一、溶質(zhì)單一型——關(guān)注三個(gè)守恒 1.弱酸溶液: 【例1】在0.1mol/L的H2S溶液中,下列關(guān)系錯(cuò)誤的是( ) A.c(H+)=c(HS-)+c(S2-)+c(OH-) B.c(H+)=c(HS-)+2c(S2-)+c(OH-) C.c(H+)>[c(HS-)+c(S2-)+c(OH-)] D.c(H2S)+c(HS-)+c(S2-)=0.1mol/L 分析:由于H2S溶液中存在下列平衡:H2S (注意:解答這類(lèi)題目主要抓住弱酸的電離平衡。) 2.弱堿溶液: 【例2】室溫下,0.1mol/L的氨水溶液中,下列關(guān)系式中不正確的是( ) A. c(OH-)>c(H+) B.c(NH3·H2O)+c(NH4+)=0.1mol/L C.c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+) D.c(OH-)=c(NH4+)+c(H+) 分析:由于氨水溶液中存在一水合氨的電離平衡和水的電離平衡,所以所得溶液呈堿性,根據(jù)電荷守恒和物料守恒知BD正確,而一水合氨的電離是微量的,所以C項(xiàng)錯(cuò)誤,即答案為C項(xiàng)。 3.強(qiáng)酸弱堿鹽溶液: 【例3】在氯化銨溶液中,下列關(guān)系正確的是( ) A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)>c(H+)>c(OH-) C.c(NH4+)=c(Cl-)>c(H+)=c(OH-) D.c(Cl-)=c(NH4+)>c(H+)>c(OH-) 分析:由于氯化銨溶液中存在下列電離過(guò)程:NH4Cl=NH4++Cl-,H2O 4.強(qiáng)堿弱酸鹽溶液: 【例4】在Na2S溶液中下列關(guān)系不正確的是 A. c(Na+) =2c(HS-) +2c(S2-) +c(H2S) B.c(Na+) +c(H+)=c(OH-)+c(HS-)+2c(S2-) C.c(Na+)>c(S2-)>c(OH-)>c(HS-) D.c(OH-)=c(HS-)+c(H+)+c(H2S) 解析:電荷守恒:c(Na+) +c(H+)=c(OH-)+c(HS-)+2c(S2-); 物料守恒:c(Na+) =2c(HS-) +2c(S2-) +2c(H2S); 質(zhì)子守恒:c(OH-)=c(HS-)+c(H+)+2c(H2S),選A D 5.強(qiáng)堿弱酸的酸式鹽溶液: 【例5】(2004年江蘇卷)草酸是二元弱酸,草酸氫鉀溶液呈酸性,在0.1mol/LKHC2O4溶液中,下列關(guān)系正確的是(CD) A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+ c(C2O42-) B.c(HC2O4-)+ c(C2O42-)=0.1mol/L C.c(C2O42-)>c(H2C2O4) D.c(K+)= c(H2C2O4)+ c(HC2O4-)+ c(C2O42-) 分析:因?yàn)椴菟釟溻洺仕嵝裕訦C2O4-電離程度大于水解程度,故c(C2O42-)>c(H2C2O4)。又依據(jù)物料平衡,所以D.c(K+)= c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)正確,又根據(jù)電荷守恒:c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-),所以綜合上述C、D正確。
習(xí)題練習(xí) 1、(2001年全國(guó)春招題)在0.1mol·L-1 Na2CO3溶液中,下列關(guān)系正確的是( )。 A.c(Na+)=2c(CO32- B.c(OH-)=2c(H+) C.c(HCO3-)>c(H2CO3) D.c(Na+)<c(CO32-)+c(HCO3-) 2、在0.1mol/L的NaHCO3溶液中,下列關(guān)系式正確的是( ) A.c(Na+)>c(HCO3-)>c(H+)>c(OH-) B.c(Na+)=c(HCO3-)>c(OH-)>c(H+) C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) 3、 已知某溫度下0.1mol·L-1的NaHB(強(qiáng)電解質(zhì))溶液中c(H+)>c(OH-),則下列有關(guān)說(shuō)法或關(guān)系式一定正確的是( ) ①HB-的水解程度小于HB-的電離程度;②c(Na+)=0.1mol·L-1 ≥c(B2-); ③溶液的pH=1;④c(Na+)=c(HB-)+2c(B2-)+c(OH-)。 A.①② B.②③ C.②④ D.①②③ 4、(2006江蘇)1、下列敘述正確的是( ) A.0.1mol·L-1氨水中,c(OH-)=c(NH4+) B.10 mL 0.02mol·L-1HCl溶液與10 mL 0.02mol·L-1Ba(OH)2溶液充分混合,若混合后溶液的體積為20 mL,則溶液的pH=12 C.在0.1mol·L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) D.0.1mol·L-1某二元弱酸強(qiáng)堿鹽NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) 5、(05上海)14、疊氮酸(HN3)與醋酸酸性相似,下列敘述中錯(cuò)誤的是( ) A、HN3水溶液中微粒濃度大小順序?yàn)椋篶(HN3)>c(H+)>c(N3ˉ)>c(OHˉ) B、HN3與NH3作用生成的疊氮酸銨是共價(jià)化合物 C、NaN3水溶液中離子濃度大小順序?yàn)椋篶(Na+)>c(N3ˉ) >c(OHˉ)>c(H+) D、N3ˉ與CO2含相等電子數(shù) 本文由公眾號(hào)《向?qū)W霸進(jìn)軍》整理編輯 |
- 關(guān)注天氣: